BCS people
- 작성자 Admin
- 작성일 2025.02.28
- 조회수 1685

최민이 교수님 minee.choi@kaist.ac.kr https://mineechoilab.kaist.ac.kr/
2006. 한양대학교 의과대학 의학석사
2013. 영국 케임브리지 대학교 임상 신경과학 박사 졸업 (PI: Roger Barker)
2013~2022. 런던 대학교 UCL 박사후 연구원 (PI: Sonia Gandhi)
2017~2022 런던 크릭 연구소 파견 연구원
2023.2~ 카이스트 뇌인지과학과 조교수
Q1. 어떤 연구를 하시는지 간단히 소개해주세요.
저는 뇌 오가노이드(organoid)를 이용해서 뇌질환을 연구하고 있습니다. 알츠하이머 병, 파킨슨 병, 루이 소체 치매와 같이 많은 사람들에게 고통을 주고 있는 질환의 원인을 밝혀내고 효과적인 치료법을 개발하는 것이 목표죠.
- 뇌 오가노이드라면 요새 굉장히 핫한 분야라고 알고 있어요. 구체적으로 무엇인지, 왜 그렇게 인기 있는지 자세히 설명해주실 수 있나요?
저도 처음부터 오가노이드를 활용했던 건 아니에요. 박사 과정 때는 동물 모델과 배아 줄기 세포를 이용했죠 정자와 난자가 만나 만들어진 수정란이 세포 분열을 거듭하다 보면 배반포(blastocyst)라는 세포 덩어리가 생기는데, 그 덩어리의 내막 (inner cell mass)에서 다양한 세포로 분화할 수 있는 능력을 가진 배아 줄기 세포(embryonic stem cell)를 얻을 수 있어요. 한때는 그게 줄기 세포를 얻을 수 있는 유일한 방법이라 생각되었었죠. ‘생물학적 과정은 역전될 수 없다’는 게 학자들의 공통된 믿음이었으니까요.
그런데 2012년에 노벨 생리의학상을 받은 야마나카 신야, 존 거든 교수가 유도 만능 줄기 세포(induced pluripotent stem cell)라는 혁신적인 발명을 해내요. 그분들은 줄기 세포와 다른 세포를 면밀히 비교해서 줄기 세포에 보다 많이 존재하는 물질의 리스트를 만들었습니다. 수백 개의 리스트 중에서 아주 핵심적인 역할을 하는 물질 4개를 추려냈고, 그 4개를 적절하게 넣어주면 성체 세포를 줄기 세포로 되돌릴 수 있다는 걸 알아냈어요. 비유하자면, 30대 성인에게 4종의 특수 약물을 먹였더니 나이를 거꾸로 먹어 신생아로 돌아간 거죠. 그렇다고 세포 모양이 배아 줄기 세포처럼 변하는 건 아니지만, 그것이 가진 가장 핵심적인 능력인 ‘분화 가능성’을 띠게 됩니다.
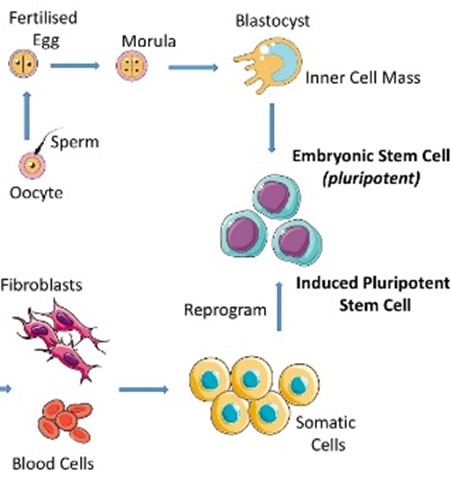
▲배아 줄기 세포(embryonic stem cell)와 유도 만능 줄기 세포(induced pluripotent stem cell)를 만드는 과정을 설명한 그림 (출처: https://www.frontiersin.org/journals/bioengineering-and-biotechnology/articles/10.3389/fbioe.2020.597661/full)
분화 가능성이 있다는 건 뇌세포로도 분화될 수 있다는 뜻이죠. 이를 이용해서 포스닥 때 제가 한 연구가 환자 유래 줄기세포를 만드는 것이었습니다. 뇌질환을 연구하려면 해당 질환을 앓는 사람의 뇌세포가 필요한데, 아픈 사람에게 뇌를 열어서 세포를 떼달라 할 수는 없잖아요. 대신 피부 세포나 혈액 샘플을 채취한 다음 아까 말한 4종의 물질을 써서 줄기 세포 상태로 되돌리고 이걸 잘 키워 뇌세포를 만들어요. 신경세포(neuron) 뿐만 아니라 별아교세포(astrocyte), 미세아교세포(microglia) 같은 신경교세포(glial cell)까지 키워내 실제 뇌에 존재하는 세포를 비슷하게 재현해내죠. 이렇게 만든 미니 뇌를 뇌 오가노이드라고 합니다.
이 오가노이드가 있으면 다양한 분석을 통해 환자 뇌의 고유한 특징을 파악할 수 있고, 개발한 약물을 테스트해볼 수도 있죠.
- 김철수 씨 세포에서 키운 뇌 오가노이드, 박영희 씨 세포에서 키운 뇌 오가노이드…. 하는 식으로, 다 다른 오가노이드가 만들어지는 거군요.
그렇죠. 같은 질병을 앓고 있더라고 사람마다 뇌의 특징이 다르고 증상이 다르기 때문에 오가노이드별로 약물을 테스트하면서, ‘이 환자에게는 이 약물이 잘 듣겠구나’ ‘이 환자는 이 약물 독성에 취약하구나’ 같은 정보를 알아낼 수 있어요.
연구하는 질병별로도 오가노이드가 달라지는데, 뇌의 모든 부위를 재현한다면 참 좋겠지만 현실적으로 어렵기 때문에 질병과 가장 관련이 깊은 영역을 부분적으로 만들고 있습니다. 파킨슨병의 경우 중뇌(midbrain)이 가장 중요하기 때문에 중뇌 오가노이드를 중점적으로 키워내죠. 거기에 더해 다른 곳으로 뻗는 회로를 보고 싶으면 억제성 신경 세포를 추가하고, 대뇌 피질과 연결성을 보고 싶으면 대뇌 피질 영역 세포를 추가하는 식으로 효율적으로 만들어냅니다.
- 그럼 현재 누구에게서 세포를 얻어 오가노이드를 만들고 계시나요?
제가 직접 환자를 만나 세포 샘플을 떼오는 건 아니고요, 그렇게 해서 만든 유도 만능 줄기 세포를 공유하는 센터가 있어요. 일종의 줄기 세포 은행 같은 거죠. 안타깝게도 한국에는 존재하지 않아 영국의 EBiSC나 미국의 NINDS 같은 센터에 요청해서 가져오고 있는데, 그러기까지의 서류 과정이 굉장히 복잡해서 많은 연구실들이 수입을 하지 못하고 있는 상황이에요. 파킨슨 병 환자에게서 추출한 유도 만능 줄기 세포를 센터에서 들여오는 것은 국내에서 제가 최초랍니다.
- 오가노이드 키우는 게 어렵진 않나요? 저는 학부 시절 연구실 인턴을 하면서 세포 배양 실험을 몇 번 해봤는데, 단순히 세포인데도 꽤 까다로웠거든요. 배지도 계속 갈아줘야 하고, 잘못 만지면 죽어버리고….
어렵죠. 요리로 비유하자면 레시피만 안다고 되는 게 아니라 경험에서 나오는 노하우가 있어야 해요. 김장을 하려 하는데 요리책에 소금에 24시간 재우라고 적혀 있었다고 쳐요. 그런데 올해 날씨가 너무 안 좋아서 배추가 딱딱하게 나왔다면, 24시간이 아니라 그보다 좀 더 재워야 하잖아요. 그처럼 정해진 프로토콜을 잘 따라한다고 해서 잘 키울 수 있는 게 아니고 그때그때 오가노이드의 상태를 파악해서 적절한 조치를 취해줘야 해요.
- 들어온지 얼마 안 된 학생들은 많이 죽일 것 같은데요.
많이 죽어요. 오가노이드는 연약하고 예민한 아기 같은 존재거든요. 특히 유도 만능 줄기 세포는 원래 성인 세포였는데 억지로 나이를 되돌려서 어린 상태로 만든 거기 때문에 그 상태를 유지하는 것만으로도 엄청난 에너지를 써요. 그런데 그걸 다시 분화시켜 뇌세포로 만들기까지 해야 하니 까다로울 수밖에 없죠. 더군다나 건강한 세포도 아니닌 질병에 걸린 환자의 세포니까요. 많이 실패하고 많이 죽이면서 노하우를 터득하게 돼요. 1만 시간의 법칙을 믿으라고 학생들에게 이야기합니다.
Q2. 의대를 졸업하셨는데, 어떻게 의사가 아닌 학자의 길을 걷게 되셨는지 궁금합니다.
2학년 때 신경생리학 수업을 듣다 신경 세포의 활동 전위(action potential)라는 개념에 반해 버렸어요. 그전까진 이해도 못 하고 지루하다 생각하던 주제였는데, 교수님이 이온의 전기화학적 농도부터 막전위까지 차근차근 설명해주시니까 암기만 하고 있던 것들이 갑자기 전부 이해되면서 너무 재미있는 거예요. 수업이 끝나고 그 교수님을 찾아가서 ‘평생 이것만 공부하며 살고 싶어요’ 했더니, 교수님께서 저를 앉혀 두고 병원에서 의사로 일하는 것과 연구실에서 학자로 일하는 게 얼마나 다른지 설명하셨어요. 의사는 퇴근하면 그날 일이 끝나는 거지만, 학자는 집에서 TV 보면서도, 밥 먹으면서도 연구 생각을 해야 한다고요. 저는 정확히 그렇게 살고 싶었어요. ‘의학 연구’라고 학생들이 다들 싫어하던 프로젝트 과목이 있었는데, 저는 도서관 가서 책 찾고 활동 전위 공부하는 게 너무 좋아서 확신을 가지게 됐죠. 결국 졸업 후 활동 전위를 설명해주신 그 교수님 밑으로 들어가 석사를 했습니다. 국내는 아직까지 의학 연구를 하기 어려움이 많다고 하셔서 박사는 영국으로 유학을 가게 됐고요.
Q3. 그 뒤로 영국에서 오래 공부하셨는데, 영국 대학에 교수로 부임하지 않고 한국으로 오신 이유가 궁금해요.
영국 박사는 대체로 4년 과정이고, 그 후 졸업 논문을 쓰는 기간이 1년 정도 주어져요. 리뷰어들에게 제출한 뒤 검사 받고, 교정해서 재제출하면서 또 1년이 갑니다. 그동안 다른 연구실에서 비공식 포스닥처럼 일하는 게 보통이고요. 졸업한 후 research fellow로 일하고, 평균적으로 8년차에 early career가 끝나서 교수직에 지원하죠. 그때까지만 해도 한국에 돌아갈 생각은 없었는데, 운명처럼 카이스트에 뇌인지과학과가 생겼다는 소식이 들려온 거예요. 친구 하나가 ‘여기 너를 위한 데인 것 같아’라며 링크를 보내줬는데, 여기라면 뇌과학 연구를 부족함 없이 할 수 있겠다 싶어서 지원했죠. 그렇게 카이스트 뇌인지과학과 창립 멤버가 되었습니다. 학과의 설립부터 발전까지 전부 겪고 있어요.
Q4. 학과 설립 이래 약 2년이 지났는데, 그동안 어떤 일을 하셨나요?
연구실 셋업과 세포 샘플 확보를 위한 협력처 탐문에 가장 많은 시간을 쏟았어요. 제 연구에는 환자에게서 추출한 세포 샘플이 꼭 필요한만큼 부임하자마자 샘플을 공급받을 수 있는 곳을 찾아 나섰는데, 국내에서는 찾을 수가 없었어요. 질병으로 고통받고 있는 환자에게 치료도 아니고, 언제 성공할지 모르는 연구 목적으로 세포를 달라고 하는 게 쉽지 않은 일이거든요. 범위를 아시아로 넓혀 찾아보다 대만의 장경기념병원(長庚記念醫院)을 알게 됐어요. 1만 2천개의 병상을 가진 아시아에서 가장 큰 병원인데, 상호 이해가 잘 맞아떨어져 올해 학교 차원에서 그곳과 MOU를 맺었습니다. 병원에서 환자의 세포와 더불어 의사가 관찰한 환자의 임상 데이터를 보내주면, 우리가 세포를 바탕으로 오가노이드를 만들고, 그럼 환자의 병리적 특성과 환자 세포로 만든 뇌 오가노이드의 생물학적 특성을 비교할 수 있는 거죠. 아시아에서는 전례가 없던 시스템이에요. IRB 승인도 끝났고, 실현을 눈앞에 두고 있습니다. 빨리 환자 데이터를 받아서 연구하고 싶어요.

▲장경기념병원을 설립한 포모사(Formosa) 그룹의 회장 샌디 왕(王瑞瑜)이 올해 5월 KAIST에 방문했을 때의 사진. 관련 기사: ‘KAIST, 대만 포모사그룹과 본격적인 협력 시작하다’ (카이스트 뉴스, 2024.5.9) https://researchnews.kaist.ac.kr/researchnews/html/news/?mode=V&mng_no=36690
Q5. 연구자로서 앞으로 카이스트에서 이루고 싶은 목표는 무엇인가요?
반드시 이루고 싶은 목표는 병을 치료하는 것이에요. 현재까지 개발된 치료제는 근본적으로 질환을 해결하는 것이 아니라, 증상을 완화하는 용도니까요. 특히 파킨슨 병은 스펙트럼이 워낙 넓어서 모든 사람에게 듣는 치료제가 존재하지 않아요. 세부 유형에 걸맞는 걸 써야 하는데, 그 세부 유형이 너무 많다보니 치료가 까다롭죠. 환자 맞춤 오가노이드 연구를 통해 분자생물학에 의거한 진단을 내리고, 세부 유형을 정확히 파악한다면 파킨슨병의 정복도 불가능한 일이 아니라 믿습니다. 과거에는 저주받은 병이라 여겨졌지만 현재는 완벽한 치료제가 개발된 한센병처럼, 인류는 이미 불치병이라 생각했던 질환을 고친 경험이 있으니까요.
- 교수자로서의 목표는요?
완치를 내 생에 못하면 제자들이 할 수 있도록…. (웃음) 나는 파킨슨 병을 타겟으로 했지만, 세상에는 아주 많은 뇌질환이 있으니 제자들이 다양한 질병에 대해 세부 유형을 분류하고 각각에 대한 약물을 개발했으면 좋겠어요. 특히 정신과적 질환 중에서는 효과적인 치료제가 없다시피 한 병이 많거든요, 조현병처럼.
- 정신과적 질환의 치료제를 개발하는 데도 오가노이드가 유용하게 사용될 수 있을까요? 우울증, 조현병 같은 병은 증상이 인지적인 것이잖아요.
증상은 인지적이지만, 그 기저에는 생물학적 원인이 존재해요. 예를 들어, 활동 전위가 발생해 신경 세포 내부로 칼슘이 유입되면 세로토닌 같은 신경전달물질이 시냅스에서 방출되는데요. 환자의 경우 정상적인 칼슘 농도 조절이 잘 이루어지지 않아요. 자극에 반응하는 속도도, 반응한 후 원래대로 돌아오는 속도도 정상인에 비해 느리죠. 이런 것들을 오가노이드로 구현할 수 있는 거고요.
파킨슨 병의 경우에도 현재 가장 널리 쓰이는 치료제인 리보도파를 투여하면 부작용으로 환각이 나타나는 일이 잦아요. 이럴 때 환자의 뇌를 열어 뭐가 문제인지 검사해볼 수 없으니, 오가노이드를 만들어 조사하면 도움이 되겠죠.
Q6. 학부생을 대상으로 ‘동물 신경 해부학 및 신경 생리학 실습’ 강의를 진행하고 계신데요. 구체적으로 무엇을 실습하는 강의인가요?
기본적으로 동물 뇌를 보는 수업이에요. 우리가 동물 뇌를 연구하는 이유는 궁극적으로 사람 뇌를 알기 위해서이기 때문에, 비교 해부학적 강의의 성격도 띠죠. 실습은 쥐의 뇌를 가지고 하되 실습하기 전 VR로 사람 뇌를 해부하는 활동이 포함되어 있습니다. 시뮬레이션 프로그램 상에서 사람 뇌를 가지고 전압을 조작하거나, 저항을 바꿔보면서 활동 전위가 어떻게 바뀌는지 관찰하도록 했어요.
fNIRS (functional near-infrared spectroscopy. 근적외선을 사용하여 뇌의 혈류량을 측정하는 원리로, 뇌의 영역별 활성도를 파악할 수 있는 비침습적인 기술) 실습도 한 적 있는데요, 학생들에게 수학 문제를 풀게 하고 뇌의 활성도를 관찰해보았더니 대체로 활성화가 잘 안 된다는 흥미로운 결과가 나왔어요. 너무 익숙한 활동이다보니 뇌를 열심히 굴리지 않아도 문제가 풀리는 거죠.
Q7. 2016년부터 Journal of Alzhemier’s and Parkinson’s Dementia의 편집 위원으로 활동하고 계시다고 들었어요. 편집 위원으로서 어떤 일을 하시나요?
주 업무는 논문의 리뷰를 관리하는 것입니다. 투고된 논문의 주제에 걸맞는 연구자를 찾아 리뷰 업무를 맡기는 것이죠. 보통 논문을 투고받으면 원고를 읽으면서 키워드를 정리하고, 해당 키워드로 검색해서 비슷한 연구를 하는 사람들을 찾아봐요. 요즘은 투고한 사람이 ‘위시 리뷰어’와 ‘블랙리스트 리뷰어’, 즉 내 논문을 리뷰 해줬으면 하는 사람과 안 해줬으면 하는 사람 명단도 같이 보내기 때문에 그것도 참고하고요. 저는 논문을 리뷰하고 수정하고, 반박하는 과정을 즐거워하는 편이라 포스닥 때부터 꾸준히 하고 있는 작업입니다.
Q8. 자유롭게 연구실 홍보 부탁드립니다.
즐겁게 연구할 수 있는 환경을 만들고자 합니다. 내가 학생들에게 연구를 시키는 게 아니라, 학생들에게 자유를 주고 본인이 하고 싶은 연구를 즐겁게 할 수 있도록 노력하고 있어요. 성숙한 개인주의 문화를 바탕으로 자유로운 출퇴근과 재택 근무를 실행하고 있고요. 단체 랩미팅 대신 지도교수와 깊고 솔직한 이야기를 나눌 수 있는 1:1 랩미팅을 정기적으로 하고 있는데, 덕분에 학생들이 다른 학생들 앞에서는 하기 어려웠을 이야기, 고민 등을 솔직하게 털어놓아요. 또, 학과 창립과 함께 만들어진 연구실인만큼 후에 합류한 연구실에 비해 셋업이 많이 진행된 상태라는 것도 장점입니다. 처음 들어온 두 학생이 열심히 일해준 덕분에 평균보다 빠르게 자리잡을 수 있었어요. 물리학, 심리학, 생명과학, 생명공학 등 다양한 백그라운드의 학생들이 있으니 연구 분야에 관심이 있다면 적극적인 지원 바랍니다.
